REDOXREACTIES
Inleiding
Het onderwerp van deze module is "REDOX-reacties", waarbij REDOX het resultaat is van afkortingen:
RED komt van Reductor
OX komt van oxidator
In elke redoxreactie zijn dat de twee belangrijke deelnemers.
In een redoxreactie reageren altijd een oxidator en een reductor
en opgelet:
Er ontstaan daarbij ook altijd een nieuwe oxidator en een nieuwe reductor
Je zou een beetje ijzerpoeder en zwavelpoeder goed moeten mengen in een reageerbuis en voorzichtig verhitten boven een brandervlam.
Eerst smelt het zwavel en met dat ijzerpoeder erin lijkt het dan een zwart vloeibaar mengsel te worden, maar al gauw gaat het echt reageren.
Het gaat zelfs gloeien, zo veel energie komt er bij vrij.
Het resultaat - je kunt dat na afkoelen gewoon vastpakken - is een harde, vormloze substantie, zwart van kleur
en lijkt helemaal niet meer op ijzer of zwavel.
We hebben hier een voorbeeld van een redoxreactie met ijzer als reductor en zwavel als oxidator.
Wat is er precies gebeurd?
Een korte herinnering aan scheikundige begrippen die je hier nodig hebt:
Redox heeft alles te maken met elektronen, meestal de valentie-elektronen van bepaalde atomen.
Hoe zit dat ook weer met het afgeven en opnemen van elektronen?
Je weet vast nog:
Alle deeltjes (atomen, moleculen, ionen, ze bevatten altijd elektronen.
Opdracht 1
Schrijf precies op wat er gebeurt als twee deeltjes elkaar tegenkomen en één wil elektronen afgeven en de ander wil opnemen.
Opdracht 2
Hoeveel elektronen bevinden zich in de volgende deeltjes:
Ba2+ SO42- 6C6H12O6 U
Antwoord 10-02
Inhoud van de module
1. Redoxreactie
1.1 Definities
1.2 Redoxkoppel
1.1 Redox-halfreactie
1.2 Redox-evenwicht, zwak en sterk
2. Directe Redoxreacties
2.1 Redoxreactievergelijkingen
2.2 Metalen & Corrosie
2.2 AutoRedox
3. Indirecte Redoxreacties; met elektroden
3.1 Het gebruik van elektroden
3.2 Batterijen en accu's
3.1 Elektrolyse
3.2 Elektrodepotentiaal
4. Oxidatiegetal
5. Oplossen van redoxreacties
6. Toepassingen
6.1 Alkoholtest
6.1 Fotografie
Een redoxreactie is een chemische reactie waarbij elektronen worden overgedragen van de reductor naar de oxidator
Een oxidator is een deeltje dat elektronen kan / 'wil' opnemen;
Hij is een elektronenacceptor
[n.b.: dat 'wil' staat tussen aanhalingstekens, omdat 'iets willen' eigenlijk niet iets is van materie.
Materiedeeltjes hebben geen vrije wil.
Wellicht hebben levende wezens dat wel, maar zeker is dat niet.
Maar toch gebruiken we in deze cursus nu en dan dit soort woorden, gewoon omdat het ook wel leuk is net te doen alsof stoffen iets willen of niet willen.
Bovendien, we weten heus nog niet alles van de materie.]
Een reductor is een deeltje dat elektronen kan / wil afstaan;
Hij is een elektronendonor
Elektronen zijn niet los verkrijgbaar. Ze horen altijd bij één of meerdere deeltjes.
Overdracht van elektronen, normaliter, gebeurt niet op afstand, alleen in direct contact tussen twee deeltjes.
Een reductor kan dus niet een elektron 'afschieten' en even verderop de oxidator 'raken'.
[Even tussendoor: iemand met een beetje verstand van scheikunde moet in elk geval snel en gemakkelijk een behoorlijk aantal formules direct herkennen als reductor of oxidator.]
Er zijn een paar regeltjes ontdekt die gelden voor stoffen / deeltjes die aan een redoxreactie meedoen:
- Er zijn oxidatoren en reductoren die uitsluitend reageren als er ook nog bepaalde andere (hulp)stoffen aanwezig zijn.
- van de neutrale elementen zijn vooral een aantal niet-metalen heel vaak oxidatoren
- van de neutrale elementen zijn vooral een aantal metalen heel vaak reductoren
Bovenstaande vuistregels hebben alles te maken met het feit dat metaalatomen maar weinig valentie-elektronen hebben en niet-metalen veel.
Om dit te bestuderen moet je naar module 03 over chemische bindingen en naar module 01 over de atoombouw.
Opdracht 3
- Roep tabel X op om halfreacties te zien.
- Haal alle neutrale metalen er uit en noteer die in volgorde van sterkte.
- Litium is de sterkste reductor en goud de zwakste. Controleer dat.
- Let wel: alleen die metalen die geen hulpstoffen, zoals bijvoorbeeld H+, nodig hebben volgens de tabel.
- En kijk, nu heb je de zgn. spanningsreeks van metalen te pakken.
- Vervolgens kun je hetzelfde doen voor de niet-metalen, onder uitsluiting van degene die hulpstoffen nodig hebben.
Opdracht 4
Kies het juiste antwoord:
Zuurstof kan glucose volledig oxideren. De producten van deze volledige oxidatie zijn:
- Zuurstof en waterstof
- Kooldioxide en water
- Kooldioxide en ureum
- Uitsluitend water
Heel veel redoxreacties komen we in de praktijk tegen, ook in het dagelijks leven, zoals het verbranden van brandstoffen als benzine met zuurstof, of het roesten van ijzer, maar ook de energieproductie in het menselijk lichaam. Allemaal verbrandingsreacties.
Toch zullen de meeste redoxreacties van deze cursus niet zozeer verbrandingsreacties zijn.
Ook in het dagelijks leven zijn er, behalve zuurstof, nog zoveel meer oxidatoren (en ook reductoren): ijzer, glucose, permanganaat, waterstof, alcohol, enzovoort.

Opdracht 5
Leg uit of de volgende stoffen oxidator of reductor zijn: Zuurstof, ijzer, glucose, permanganaat, waterstof.
Opdracht 6
Leg uit of de volgende beweringen waar of onwaar zijn:
- Een stof die als oxidator fungeert, moet het element zuurstof bevatten
- De reactie:
IJzer(s) + Koper(II)sulfaat(aq)  Koper(s) + IJzer(II)sulfaat(aq)
Koper(s) + IJzer(II)sulfaat(aq)
is een redoxreactie.
In de geschiedenis van de chemie is ontwikkeling geweest in het definiëren van wat oxidater en reductor zijn.
Aanvankelijk koppelde men het woord oxidator aan het element 'oxigenium' (zuurstof), maar vandaag de dag kennen we vele oxidatoren die niets met zuurstof te maken hebben.
We gebruiken andere definities dan vroeger.
Opdracht 7
Schrijf eens voor jezelf op, zonder verder te kijken in deze cursus, hoe je een redoxreactie zou definiëren.
Wat is jou formulering?
Opdracht 8
Welk antwoord is juist? Leg uit:
Tijdens de oxidatie van glucose zullen de moleculen van glucose:
- elektronen verliezen
- H+ ionen verliezen
- H+ ionen ontvangen
- elektronen ontvangen
Meer definities:
Een redoxreactie is een chemisch proces
waarin elektronen worden overgedragen van de ene stof naar de andere.
of anders:
Een redoxreactie is een chemisch proces
waarin de oxidatiegetallen van één of meer elementen veranderen.
[Verderop meer over oxidatiegetallen]
Een stof die tijdens een reactie elektronen wint of krijgt noem je een oxidator (Ox)
Het omgekeerde: een stof die elektronen verliest is een reductor (Red)
Tijdens een redoxreactie reageren altijd een reductor en een oxidator met elkaar
er worden elektronen overgedragen van de reductor naar de oxidator.
Bij deze overdracht betreft het vrijwel altijd elektronen uit de buitenste elektronenschil van de atomen (valentie-elektronen) die aan de reactie deelnemen.
Opdracht 9
Probeer terug te halen wat ook weer een elektronenformule is en geef wat voorbeelden.
Het antwoord op opdracht 9 komt hier al zo ongeveer:
Een elektronenformule toont alle valentie-elektronen in de vorm van streepjes of puntjes (één streepje = twee puntjes).
Als elektronenformules veranderen tijdens een reactie moet er sprake zijn van overstap / overdracht van elektronen,
dus is het een redoxreactie.
Een paar voorbeelden:
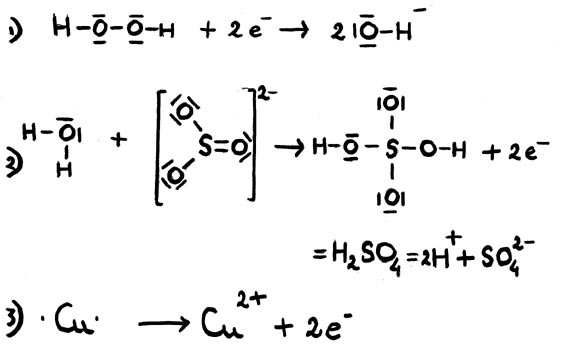
In middelste voorbeeld geeft een zwavelatoom twee elektronen af en dient dus als reductor, waarbij sulfaat ontstaat uit sulfiet
Opdracht 10
Bij het roesten van ijzer is het ion ijzer(III) een product.
- Wie is hierbij oxidator of / en reductor?
- Wat gebeurt er met de valentie-elektronen?
- Geef de halfreactie en wat is het 'redoxkoppel'?
Een redoxreactie is altijd opgebouwd uit twee halfreacties:
| De vergelijking van koppel 1: |
red 1 |
 |
ox 1 + elektronen |
| vergelijking van koppel 2: |
ox 2 + elektronen |
 |
red 2 |
| Totaalvergelijking: |
red 1 + ox 2 |
 |
ox 1 + red 2 |
Het aantal elektronen dat betrokken is bij een redoxreactie moet voldoen aan de regel:
ER WORDEN EVENVEEL ELEKTRONEN AFGEGEVEN ALS OPGENOMEN
Elektronen gaan nu eenmaal niet verloren en ook komen ze niet uit het niets tevoorschijn, en daarom:
Altijd moet je de twee halfreactievergelijkingen zodanig kloppend maken dat het aantal afgegeven elektronen gelijk is aan het aantal opgenomen elektronen.
Voorbeeld:
| De vergelijking van koppel 1: |
Al |
 |
Al3+ + 3e- |
| x 2 |
| vergelijking van koppel 2: |
I2 + 2e- |
 |
2I- |
| x 3 |
| Totaalvergelijking: |
2Al + 3I2 |
 |
2Al3+ + 6I- |
De totaalreactie is alleen betrouwbaar als het aantal elektronen dat halfreactie 1 afstaat gelijk wordt gemaakt aan het aantal elektronen dat halfreactie 2 opneemt.
Voor het geval het zout aluminiumjodide onoplosbaar is, zal er sprake zijn van een vervolgreactie: de neerslagvorming van een onoplosbaar zout.
Let op: dat is hier niet het geval; controleer dat in tabel XI: oplosbaarheid van zouten in water.
Opdracht 11
Plaats een ijzeren spijker in een oplossing van koper(II)sulfaat.
De blauwe kleur van de koper(II)-ionen wordt dan lichter, kan zelfs verdwijnen, en er vormt zich een nieuwe vaste stof in het reactievat.
Geef de twee redoxkoppels en de beide vergelijkingen van de halfreacties.
We hebben weer tabel X nodig met de redoxkoppels, waar we een kolom met reductoren en een met oxidatoren tegenkomen.
Naast elkaar staan telkens de bij elkaar behorende (geconjugeerde) deeltjes.
Welk boek over scheikunde dan ook, altijd is er wel een redoxtabel, haast altijd wel met wat verschillen onderling,
bijvoorbeeld waar de reductoren en oxidatoren staan, waar de sterke en waar de zwakke stoffen staan.
Let dus altijd goed op.
Opdracht 12
Oxidatoren en reductoren komen voor in de vorm van atoom, molecuul of (complex) ion.
Zoek in tabel X één voorbeeld van elk (dus drie verschillende oxidatoren en drie verschillende reductoren;
schrijf ook hun halfreacties op.
Antwoord 10-12
Veel oxidatoren en reductoren functioneren pas in aanwezigheid van bepaalde hulpstoffen.
Zo is, bijvoorbeeld, sulfaat pas in staat tot oxideren in aanwezigheid van zuur (ion H+).
Opdracht 13
Kies nog een voorbeeld van een oxidator en van een reductor die hulpstoffen nodig hebben, uit tabel X;
en schrijf hun halfreacties op.
Eenzelfde deeltje (dezelfde stof) kan in de redoxtabel meerdere keren voorkomen, dat wil zeggen, op verschillende hoogte, ofwel, in sterkte variërend.
Let op: dit verschijnsel doet zich alleen voor bij gebruik van verschillende hulpstoffen.
In principe zal altijd de sterkste reageren, maar natuurlijk onder voorwaarde dat de benodigde hulpstoffen ook echt aanwezig zijn.
Opdracht 14
Permanganaat verschijnt in sommige tabellen wel drie keer in de kolom met oxidatoren, elke keer onder verschillende condities.
Wat zal de halfreactie zijn die men gebruikt in geval van een eenvoudige oplossing van alleen kaliumpermanganaat?
Taakje apart:
Een beetje scheikundige kent haast alle stoffen uit de redoxtabel uit het hoofd, niet alleen de formules, maar ook de namen.
Doe je best. Je weet dan ergens over mee te praten als de media iets beweren.
Een redoxreactie verloopt vaak in een reversibel, omkeerbaar proces, van het type 'evenwicht' (zie module 08).
Een reductor, na het afgeven van elektronen, verandert in een stof die - op zijn beurt - weer kan opnemen: een oxidator.
En een oxidator, in een redoxreactie, wordt altijd een reductor.
| koppel 1: |
red 1 |
 |
ox 1 + elektronen |
| koppel 2: |
ox 2 + elektronen |
 |
red 2 |
| Totaalvergelijking: |
red 1 + ox 2 |
 |
ox 1 + red 2 |
Wie de evenwichtsreacties (module 08) bestudeerd heeft, weet dat een evenwicht heel vaak eenzijdig aan één kant liggen (de kant van de zwakke stoffen), hetzij links hetzij rechts.
Je moet weten dat er ook sterke en zwakke oxidatoren en reductoren zijn.
Hoe sterker een oxidator, des te sterker de neiging van deze oxidator om elektronen op te nemen.
en natuurlijk ook:
Hoe sterker een reductor, des te sterker de neiging van deze reductor om elektronen af te staan.
In de tabellen zijn de oxidatoren en reductoren geordend naar sterkte.
Opdracht 15
Vergelijk tabel X met redoxtabellen in scheikundeboeken of op internet.
Controleer of ze inderdaad zijn gerangschikt naar sterkte en of dat in al de diverse tabellen gelijk is.
De redoxreactie verloopt spontaan als we sterkere stoffen samenvoegen die zwakkere stoffen kunnen vormen.
Het omgekeerde is wel mogelijk, maar slechts met behulp van externe kracht (zie verderop).
Dus, wel of niet spontaan houdt direct verband met de sterkte van de reagentia.
In het algemeen mogen we zeggen dat een redoxreactie een evenwicht is:
red1 + ox2 ox1 + red2
ox1 + red2
Dit evenwicht beantwoordt aan de regels voor chemische evenwichten, bijvoorbeeld dat de sterken reageren ten gunste van de zwakken.
Oftewel, als je sterke stoffen samenvoegt, met voldoende energie, dan zal het grootste deel van die sterke stoffen verdwijnen (reageren) en daarbij verschijnen de zwakken in een spontaan proces.
Die zwakke producten houden nog wel een zwakke neiging om terug te reageren, maar - zwak als ze zijn - slagen daar niet goed in.
Je kunt ook zeggen: directe redoxreacties verlopen als je sterke stoffen samenvoegt.
Je kunt een redoxreactie voorspellen op grond van de plaats die oxidator en reductor innemen in de redoxtabel.
Algemene regel:
een redoxreactie verloopt (spontaan) als de oxidator zich boven de reductor bevindt (in tabel X)
Achter deze regel gaat iets anders schuil:
Als de oxidator zich boven de reductor bevindt, zullen de producten (aan de andere kant van de tabel) de zwakkere zijn.
En we weten dat die in een evenwicht overblijven.
Opdracht 16
- Controleer nu of jodium spontaan zal reageren met lood, ja of nee.
- Indien ja, kan deze reactie dan bevorderd worden met hulpstoffen?
- Welke hulpstoffen zijn dat?
Het overdragen van elektronen kan op twee wijzen plaats vinden: spontaan of gedwongen
Als deeltjes reageren die graag elektronen afstaan in contact met andere deeltjes die graag opnemen, zal de redoxreactie hoogstwaarschijnlijk spontaan verlopen.
Het zal duidelijk zijn dat dit fenomeen alles te maken heeft met sterke en zwakke stoffen.
Er is nog een manier om de redoxreacties in te delen, die ook te maken heeft met de elektronenoverdracht:
directe of indirecte redoxreacties
In dit hoofdstuk gaat het over directe redoxreacties en in het volgende hoofdstuk bespreken we de indirecte redoxreacties.
Directe redoxreacties vinden plaats op het moment dat er direct contact is tussen de betrokken deeltjes.
Directe redoxreacties kunnen alleen spontaan verlopen; er bestaan geen gedwongen directe reacties.
Je kunt zwakke redoxstoffen samenvoegen, maar spontaan zal er dan vrijwel niets gebeuren.
Als bijvoorbeeld zuurstofmoleculen en benzinemoleculen elkaar ontmoeten (allebei in vrije vorm = gasvorm), kan het resultaat van deze ontmoeting zijn: een spontane redoxreactie.
In dat geval zal het elektronentransport van de benzinemoleculen naar de zuurstofmoleculen een grote verandering veroorzaken in de stoffen.
Er ontstaan nieuwe stoffen, producten.
Bindingen worden verbroken; nieuwe bindingen worden gemaakt, net zolang tot de producten (water en koolzuurgas) gevormd zijn.
Opdracht 17
De foto's hieronder tonen een reactie tussen sulfiet en permanganaat.
Kijk in de redoxtabel en geef de halfreacties.

twee vaste stoffen, natriumsulfiet en kaliumpermanganaat, lost men op in water
(één buisje met kleurloze oplossing en één buisje met paarse heldere oplossing)

Daarna voegen we van beide oplossingen ongeveer 1 ml samen in de derde reageerbuis.

(in de rechter reageerbuizen heeft men wat extra water toegevoegd om kleur en neerslag beter te kunnen zien)
Opdracht 18
Is het roesten van ijzer een directe redoxreactie? Leg je antwoord uit.
Antwoord 10-18
Secundaire reacties / vervolgreacties.
Denk er aan dat veel reacties niet meteen klaar zijn als de producten zijn gevormd.
Het is heel goed mogelijk dat er volgreacties optreden waarin producten (bijvoorbeed de nieuwe oxidator en reductor) betrokken zijn.
Het Nitraat-ion
Nitraat-ionen doen het heel goed als oxidator, onder voorwaarde dat er voldoende zuur (H+) aanwezig is.
Het nitraat heeft diverse manieren om te reageren, afhankelijk van de concentratie van datzelfde nitraat:
- Hoge concentraties Nitraat
NO3-+ 2H+ + 1 e-
 NO2 + H2O
NO2 + H2O
- Gematigde of lage concentraties nitraat
-
Met weinig zuur: NO3-+ 4H+ + 3 e-
 NO + 2H2O
NO + 2H2O
-
Met meer zuur: 2NO3-+ 12H+ + 10 e-
 N2 + 6H2O
N2 + 6H2O
- Zeer lage concentraties nitraat
2NO3-+ 10H+ + 8 e-
 N2O + 5H2
N2O + 5H2
N.B.
| N2
|
is het normale stikstofgas, kleurloos en reukloos
|
| NO + NO2
|
de 'nitreuze dampen', geelbruin, verstikkend
|
| N2O
|
een kleurloos gas, eigenlijk een soort zenuwgas.
Het veroorzaakt lachstuipen en helpt om mensen te verdoven.
Het werd uitgevonden in 1860 en toegepast, bijvoorbeeld door tandartsen.
|
Het sulfaat-ion"
Kan ook alleen als oxidator dienen (en dan behoorlijk sterk!!) onder voorwaarde dat het vergezeld wordt door een flinke concentratie aan H+.
Zwavelzuur is dus een sterke oxidator, helemaal als het geconcentreerd is en helemaal als het een verhoogde temperatuur heeft.
Opdracht 19
Het sulfaat-ion, (met H+) staat in de redoxtabel niet zo bijzonder hoog, dus niet zo sterk als je zou verwachten.
Wat kan de reden zijn voor deze positie?
Opdracht 20
Controleer de volgende (ware) beweringen, gebruik daarbij de redoxtabel en geef je commentaar:
- Chloor is een sterkere oxidator dan Broom
- Zn is een sterkere reductor dan IJzer
- Koper(II)- en zilver(I)-ionen zijn zwakke oxidatoren
- Nitraat en sulfaat reageren alleen als oxidator in zuur milieu
- Permanganaat is als oxidator veel sterker in aanwezigheid van een zuur
- Het ion Fe2+ kan beide zijn: oxidator en reductor
red 1 + ox 2  ox 1 + red 2
ox 1 + red 2
Als de reagentia (red1 en ox2)sterk zijn (sterker dan de producten ox1 en red2),
verloopt er een spontane redoxreactie, oftewel, het evenwicht gaat ver naar rechts, ten gunste van de producten.
Van red1 en ox2 blijft nauwelijks iets over en vaak wordt dan ook niet eens het evenwichtsteken (de dubbele pijlen) gebruikt.
Omdat metalen zo'n belangrijke plaats innemen in de redoxchemie, besteden we apart aandacht aan deze elementen.
Echte toepassingen van de redox komen later.


Alle metalen zijn in principe reductoren (ze hebben weinig valentie-elektronen die ze kunnen afstaan), maar ze doen het niet allemaal in gelijke mate.
Integendeel: platina en goud zijn zeer zwak, en calcium of natrium buitengewoon sterk.
Die hele zwakke metalen reageren in de praktijk vrijwel niet; ze worden ook inert genoemd. Maar die hele sterke kunnen vaak al hevig reageren als ze alleen maar met water in aanraking komen.
Tussen die uitersten heb je de overige metalen die in meer of mindere mate (met zuren) reageren.
In industriegebieden kun je soms zien dat er zure regen geproduceerd wordt aan de manier waarop metalen en kalk in de buurt worden aangetast.
Normaal moeten metalen worden beschermd tegen invloeden van water en zuren, en dat doen we met verf, olie, menie, enzovoort, allemaal om corrosie te voorkomen.
De metalen die vrijwel niet reageren noemen we vaak de "edele" en "half-edele" metalen.
Hieronder een redoxtabel die vooral metalen bevat:
Au3+ + 3e-  Au
Au
NO3- + 2H+ + e-  NO2 + H2O
NO2 + H2O
Ag+ + 1e-  Ag
Ag
Fe3+ + 1e-  Fe2+
Fe2+
Cu2+ + 2e-  Cu
Cu
Cu2+ + 1e-  Cu+
Cu+
SO42- + 2H+ + 2e-  SO32- + H2O
SO32- + H2O
Pb2+ + 2e-  Pb
Pb
Ni2+ + 2e-  Ni
Ni
PbSO4 + 2e-  Pb + SO42-
Pb + SO42-
Fe2+ + 2e-  Fe
Fe
Zn2+ + 2e-  Zn
Zn
2H2O + 2e-  H2 + 2OH-
H2 + 2OH-
Al3+ + 3e-  Al
Al
Mg2+ + 2e-  Mg
Mg
Al(OH)4- + 3e-  Al + 4OH-
Al + 4OH-
Na+ + 1e-  Na
Na
Ba2+ + 2e-  Ba
Ba
Ca2+ + 2e-  Ca
Ca
K+ + 1e-  K
K
Deze tabel gaan we een beetje analyseren:
In de kolom met oxidatoren staat het goud-ion, de sterkste oxidator met als geconjugeerde reductor het metaal goud, de zwakste reductor.
In de praktijk heeft goud niet de minste neiging tot reageren, elektronen af te staan. Het is een edelmetaal.
Algemeen gesproken mogen we zeggen dat een reactie tussen reductor en oxidator spontaan zal verlopen als in deze tabel de reductor boven de oxidator staat.
Zo zal zilver dus reageren met salpeterzuur, maar niet met zwavelzuur. En calcium reageert spontaan met water, ijzer niet.
Hierbij moeten we bedenken dat de tabellen rekening houden met standaardtemperaturen van 20 ŕ 25oC.
De positie van een stof in deze tabellen kan veranderen als de temperatuur wijzigt.
Vuistregel: voor een spontane redoxreactie moet de oxidator boven de reductor staan.
In de tabel zijn vier niet-metalen opgenomen, namelijk de vier oplossingen/ vloeistoffen: salpeterzuur, zwavelzuur en water.
Opdracht 21
Leg uit of het verstandig is aluminium in contact te laten met water.
We zien ook dat diverse metalen op twee manieren kunnen reageren: met en zonder hulpstoffen.
Bijvoorbeeld: lood reageert beter in aanwezigheid van sulfaat-ionen.
Opdracht 22
Goud en zilver reageren moeilijk. Welke stof kan daarbij helpen?
Sommige deeltjes komen we in beide kolommen van de redoxtabellen tegen.
Dat is apart, want dat wil zeggen dat ze oxidator én reductor kunnen zijn, dat ze zowel elektronen kunnen opnemen als afstaan.
Of ze het één doen of het ander hangt af van de omstandigheden en van de aanwezigheid van bepaalde hulpstoffen.
In het algemeen zal het natuurlijk zo zijn dat zo'n stof als oxidator zal reageren als het een sterke reductor tegenkomt
en omgekeerd, als reductor reageren in contact met een sterke oxidator.
Voorbeelden:
Tin en tin-ionen komen we op drie manieren tegen: Sn Sn2+ Sn4+
Sn2+ kan zowel elektronen opnemen als afstaan.
Hetzelfde geldt voor Mangaan: Mn2+ MnO2 MnO4-
In het midden staat MnO2 met oxidatiegetal van Mn: +4 (Mn4+); deze kan zowel afgeven als opnemen.
Nog gekker wordt het als één en dezelfde stof tegelijkertijd gaat reageren als oxidator en als reductor, oftewel:
de stof gaat met zichzelf reageren.
elektronen worden intern overgedragen.
Sn2+-ionen kunnen met elkaar reageren waarbij het ene ion elektronen afstaat (wordt Sn4+) aan het andere ion (wordt neutraal Sn).
Zulke bijzondere gebeurtenissen noemen we "autoredox-reacties".
Genomen uit een redoxtabel:
| Oxidator |
|
Reductor |
| H2O2+ 2H+ + 2e- |
 |
2H2O |
| O2 + 2H+ + 2e- |
 |
H2O2 |
De stof waterstof(hy)peroxide kan zowel als oxidator én als reductor optreden.
Stel je voor dat dit (H2O2) zich bevindt in waterige en aangezuurde oplossing.
Het kan dus oxidator zijn: H2O2 + 2H+ + 2e-  2H2O
2H2O
maar ook:
Het kan reductor zijn: H2O2  O2 +2H+ + 2e-
O2 +2H+ + 2e-
In de tabel staat deze oxidator boven de reductor, oftewel: de stof reageert spontaan, is sterk genoeg.
Het zal dus niet gemakkelijk zijn om waterstofperoxide lang te bewaren; oxidator en reductor zitten samen in één flesje!
Het heeft de neiging om via deze autoredox omgezet te worden in water en zuurstof.
Opdracht 23
Geef de twee halfreacties + de totaalreactie van de autoredoxreactie van de ijzer(II)ionen.
Opdracht 24
Bestudeer goed de volgende halfreacties:
| oxidatoren |
|
reductoren |
| Cu+ + e- |
 |
Cu |
| Cu2+ +2e- |
 |
Cu |
| Cu2+ + e- |
 |
Cu+ |
Welk ion staat in beide kolommen? Kan dit ion deelnemen in een autoredoxreactie? Leg je antwoord uit.
Opdracht 25
Bestudeer goed de volgende halfreacties:
| Oxidatoren |
|
reductoren |
| PbO2(s) + SO42-+ 4H+ + 2e- |
 |
PbSO4(s) + 2 H2O |
| Pb2++2e- |
 |
Pb(s) |
| PbSO4(s)+2e- |
 |
Pb(s) + SO42- |
Een ion dat in de autoredox meedoet is het ion Lood(II), dat kan 2 elektronen opnemen én 2 elektronen kan afstaan.
Deze reacties worden toegepast in Lood-accu's.
- Welke van de drie halfreacties vindt plaats in de loodaccu? Leg uit.
- Waarom is het voor de praktijk belangrijk in dit geval goed te letten op de aggregatietoestand (s) in deze halfreacties?
Naast de directe, zijn er ook indirecte redoxreacties.
Dit wil zeggen: er is geen direct contact tussen de deeltjes van de oxidator en reductor. De overdracht van de elektronen gaat via-via, meestal metaaldraden of ander geleidend materiaal.
Buitenom zorgen geleidende draden voor het elektronentransport van de RED naar de OX, zonder direct contact tussen de reagentia. Die ontmoeten elkaar niet, die botsen niet.
De halfreacties vinden plaats aan het oppervlak van elektrodes (meestal ook een metaal of grafiet).
Er zijn twee soorten indirecte redoxreacties:
- spontane indirecte redoxreacties, als sterke stoffen reageren en zwakke produceren. Deze reactie is meestal ook exotherm.
- gedwongen indirecte redoxreacties, als zwakke stoffen moeten reageren en sterke vormen. Deze zijn meestal endotherm.
In beide gevallen, oftewel bij alle indirecte redoxreacties, worden elektroden toegepast.
Hieronder zie je een schema van een eenvoudige chemische cel met koper/zink elektroden.
Bestudeer dit schema met aandacht:
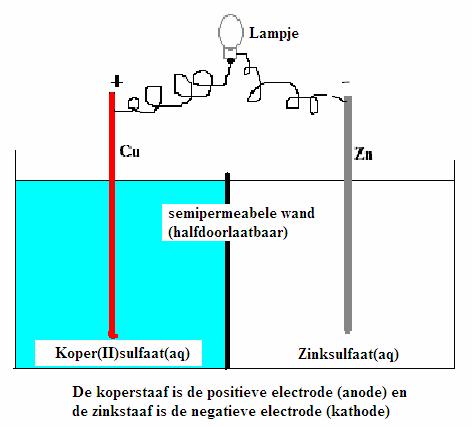
In dit complexe geheel kun je een voldoende sterke oxidator ontdekken (Cu2+) en ook een redelijk sterke reductor (Zn)
De (spontane) reacties die de boel domineren zijn:
Zn(s)  Zn2+ + 2e-
Zn2+ + 2e-
en
Cu2+ + 2e-  Cu(s)
Cu(s)
Je moet weten dat het realiseren van een redoxreactie aan het oppervlak van een elektrode vrijwel altijd een zekere activeringsenergie kost.
Zo'n reactie moet daar op gang gebracht worden.
Zeker als er bij de reactie gasvormige producten ontstaan, kan die activeringsenergie flink oplopen.
Opdracht 26
Stel je voor dat een koper(II)ion arriveert bij een elektrode, en daar een koperatoom vormt, en dat daarvoor voldoende activeringsenergie beschikbaar is,
- zal deze elektrode dan positief of negatief worden?
- Leg je antwoord uit;
- geef de half reactie;
- wat kun je waarnemen?
Indirecte redoxreacties vinden alleen plaats als er tussen de elektroden een omgeving is, een milieu, dat geleidend is voor elektrische stroom (d.w.z.: er moeten geladen deeltjes aanwezig zijn die vrij kunnen bewegen, zoals ionen van opgeloste of gesmolten zouten).
Je kunt ook zeggen dat de stroomkring bij de opstelling van een indirecte redoxreactie gesloten moet zijn. En deel van die stroomkring wordt gevormd door geleidende metaaldraden en elektroden met vrije elektronen en het andere deel wordt gevormd door een oplossing of gesmolten stof met vrije ionen.
Die vrije ionen kunnen bewegen tussen de positieve en negatieve elektrode.
Om deze beweging mogelijk te maken moeten de elektroderuimtes met elkaar in contact staan.
Dat kan met een halfdoorlatende wand (semipermeabel), of anders - als de twee elektroderuimten niet tegen elkaar aan staan - moeten die ruimten verbonden worden met een ionenbrug of beter: een zoutbrug. Dat is een soort buisje gevuld met zoutige gel (een gel met ionen).
Opdracht 27
Bestudeer het volgende schema en leg alle processen uit die daar plaats vinden.

Een elektrode kan gebrek hebben aan elektronen;
dan is die elektrode positief: anode
Een elektrode kan overschot hebben aan elektronen;
dan is die elektrode negatief: kathode
Kathode-Negatief // Anodo-Positief (KNAP)
Opdracht 28
Anionen en kationen
- Wat zijn dat?
- Hoe zijn ze geladen?
Elektroden zijn gemaakt van geleidend materiaal: meestal een metaal, soms grafiet.
Deze stoffen bevatten vrije elektronen in een metaalrooster. Deze vrije elektronen kunnen vrij bewegen binnen de elektroden,
van de negatieve naar de positieve kant = éénrichtingsverkeer).
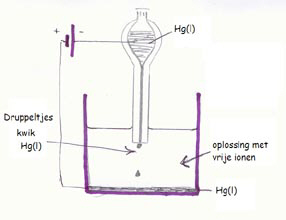
Opdracht 29
Heel bijzonder is de vloeibare elektrode. Hoe werkt die?
Kijk naar de figuur hierboven en
- leg de werking uit.
- Welke voordelen kan deze elektrode hebben?
Opdracht 30
- Leg uit waarom metalen en grafiet elektriciteit geleiden
- Leg uit waarom koper- of ijzerelektroden reageren als reductoren
- Geef een voorbeeld van een gesmolten stof die elektrische stroom kan geleiden
- Leg uit of gedestilleerd water ook elektrische stroom geleidt
Antwoord 10-30
Inerte en deelnemende elektroden:
Als het elektrodemateriaal van het type "zeer zwak" is (als reductor of oxidator stelt ie niets voor), dan zal deze elektrode INERT zijn.
Het enige dat ie doet is elektronen transporteren, maar hij neemt zelf niet deel aan de eigenlijke redoxreactie.
Voorbeelden zijn: goud, platina en grafiet.
Anderzijds gebruikt men ook elektroden die gemaakt zijn van materiaal dat echt meedoet aan de redoxreactie,
bijvoorbeeld in het geval van ijzeren of zinken elektroden.
Een ijzerstaaf kan prima als elektrode dienen, maar zal ijzer-ionen in de oplossing sturen terwijl de elektronen in de staaf achterblijven.
Het is echt zo dat een elektrode die zo gebruikt wordt, langzaamaan dunner wordt en verdwijnt.
Het ijzer ondergaat daarbij de volgende halfreactie: Fe  Fe2++2e-
Fe2++2e-
waarbij:
- Fe het ijzer is van de elektrode
- De Fe2+ -ionen de oplossing ingaan en zich vrij gaan bewegen in de richting van de negatieve elektrode
- De elektronen die achterblijven in de ijzerelektrode gaan meedoen aan de elektronenoverdracht en het elektronentransport.
Een deelnemende (dus niet inerte) elektrode is altijd gemaakt van neutrale, niet-edele metalen; ze dienen als reductoren, oftewel, ze kunnen elektronen afstaan.
Opdracht 31
- Leg uit waarom niet-metalen en elektrolyten niet kunnen dienen als elektrodemateriaal en waarom metalen en grafiet dat wel doen.
- Waarom zal het onedele metaal Natrium nooit als elektrode dienst doen in een zoutoplossing?
Opdracht 32
Leg uit waarom een deelnemende elektrode alleen kan optreden als anode en nooit als kathode.
Het woord is al een paar keer gebruikt: "elektroderuimte"; dat is de ruimte direct rondom een anode of kathode, het oppervlak incluis.
Daar vinden de halfreacties plaats bij indirecte redoxreacties.
Het kan zijn dat de kathode- en anoderuimte niet fysisch gescheiden zijn, dus dat alles plaats vindt in één oplossing of vloeistof.
Om het overal gelijk te houden wordt er soms zelf continu geroerd in de oplossing.
Maar vaak is het anders: de twee processen verlopen gescheiden en de twee elektroderuimten worden zoveel mogelijk apart gehouden,
door semipermeabele (halfdoorlatende) wanden of met zoutbruggen.
Het moet semipermeabel zijn of er moet een zoutbrug zijn; zonder dat is er geen gesloten circuit en is stroomdoorgang onmogelijk (dus ook elektronenoverdracht).
In geval van een zoutbrug moet wel gezorgd worden dat de ionen van die zoutbrug zelf niet aan de redoxreactie meedoen.
De keuze voor of tegen gescheiden elektroderuimten heeft alles te maken met wat men wil van de betreffende redoxreactie.
Apart houden heeft meestal tot doel om de produkten niet bij elkaar te brengen.
Het zou namelijk kunnen dat die producten met elkaar gaan reageren, bijvoorbeeld, een neerslag vormen of een gas.
Maar het kan ook zijn dat iemand dat juist wil.
Een oplossing (of een gesmolten stof) geleidt elektriciteit alleen onder voorwaarde van de aanwezigheid van geladen
beweeglijke deeltjes (ionen in dit geval).
De geleidbaarheid heeft alles te maken met de beweeglijkheid van die ionen: hoe beweeglijker, des te beter de geleidbaarheid.
Die beweeglijkheid, op haar beurt, hangt weer af van andere factoren:
- hoeveel ionen zijn aanwezig?
- zijn ze groot of klein of erg gehydrateerd?
- Soms heeft een ion (zeker het H+-ion in water-omgeving) nog speciale technieken om de beweeglijkheid extra te vergroten.
Opdracht 33
Leg uit waarom een metaal of grafiet niet kunnen dienen als zoutbrug.
Je mag hierbij meteen denken aan batterijen en accu's, elektrochemische cellen, galvanische elementen
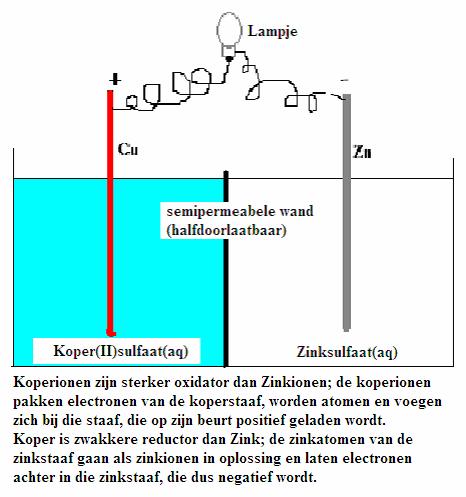
Spontane redoxreacties verlopen normaal gesproken in direct contact tussen de deeltjes van de oxidator en de reductor, maar kunnen dus ook indirect, op afstand, plaats vinden aan het oppervlak van elektroden.
Bijvoorbeeld in het geval van de reeds genoemde Cu/Zn-elektrode.
Het zink lost spontaan op, vormt Zinkionen, met achterlaten van elektronen in de zinkstaaf die daardoor negatief opgeladen wordt.
De koperionen pakken elektronen van de koperstaaf, en worden koperatomen die zich meteen samenvoegen
met de hele koperstaaf die daardoor een positieve lading krijgt.
De zink-elektrode wordt langzaam dunner en de koper-electrode zal wat groeien.
In elektrochemische cellen (galvanische elementen) vindt dus een spontane omzetting plaats van chemische energie naar elektrische energie.
Sterke stoffen reageren (oxidator en reductor), via elektroden (indirect dus), terwijl er zwakkere producten worden gevormd.
De elektronen worden getransporteerd en overgedragen via externe geleidende verbindingen (stroomdraden en elektroden).
De beweging van de elektronen door de stroomdraden heet in feite: elektrische stroom.
De toepassingen kennen we allemaal wel: batterijtjes en accu's.
Opdracht 34
Binnen de elektrochemische cel moet je altijd de elektroderuimten goed van elkaar gescheiden houden. Waarom is dat?
Bekijk de volgende evenwichten eens aan twee elektroden:
(aan de anode) red1 (Cu)  ox1 (Cu2+) + elektronen (a)
ox1 (Cu2+) + elektronen (a)
(aan de cathode) ox2 (Zn2+) + elektronen  red2 (Zn) (b)
red2 (Zn) (b)
Als een batterij stroom levert (elektronen verstuurt), komen die elektronen van de negatieve elektrode en bewegen zich buitenom naar de positieve elektrode.
Bij evenwicht (a) domineert de vorming van Koper (het evenwicht ligt links).
Zodra de elektronen bij deze pool arriveren, kan het evenwicht weer verder naar links verschuiven.
Bij evenwicht (b) domineert de vorming van zinkionen.
Zodra elektronen daar wegtrekken, probeert dit evenwicht verder te verschuiven, ook naar links.
Deze twee processen gaan geruime tijd door, net zolang tot één van de reagentia (Koperstaaf of Zinkionen) op is.
De batterij noemen we dan 'leeg'.
Een batterijtje moet dus een sterke oxidator en een sterke reductor bevatten die niet direct met elkaar mogen reageren daarbinnen.
De elektronenoverdracht moet buitenom gaan, indirect dus via stroomdraden, anders heb je er niets aan.
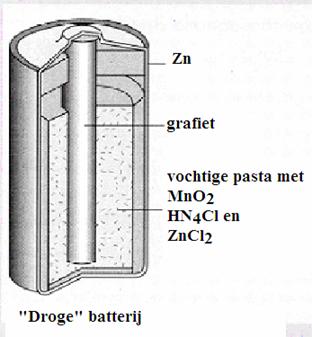
Opdracht 35
leg in eigen woorden uit (met hulp van de afbeelding) wat er in die batterij plaats vindt.
Opdracht 36
Leg uit hoe een ouderwetse auto-accu werkt (PbSO4//PbSO4/PbO2) en of je die weer kan opladen.
Opdracht 37
Controleer de redoxtabel (tabel X) en kies de oxidator en reductor met voldoende kracht om in de praktijk te dienen als elektrochemische cel (galvanisch element).
Denk je dat je zo'n element zelf zou kunnen maken?
Het is gebruikelijk dat een chemisch evenwicht zich verschuift naar de kant van de zwakke stoffen (spontane reactie).
Het kan ook anders: we kunnen een redoxreactie tussen zwakke stoffen dwingen te verlopen en daarvoor gebruiken we externe krachten:
Een stroombron die verbonden is met de elektroden in het elektrochemische systeem.
We spreken dan van elektrolyse.
Natuurlijk zijn er weer twee elektroden.
Aan één daarvan vindt de half-reactie plaats van de reductor en aan de andere de half-reactie van de oxidator.
De uitwendige stroombron heeft een positieve en een negatieve pool.
De negatieve pool verbind je met een elektrode. Wat betekent dat?
Die negatieve pool van de stroombron stuurt dan vele elektronen naar die elektrode, die daardoor dus negatief wordt (kathode).
De positieve pool van de stroombron verbind je met de andere elektrode die daardoor elektronen moet afstaan aan de stroombron en positief wordt (anode).
Deze geladen elektroden - als de lading voldoende is - gaan nu als volgt te werk:
De kathode (negatief) zal proberen elektronen kwijt te raken en zoekt naar deeltjes die elektronen willen opnemen
(dat moeten dus oxidatoren zijn)
De anode (positief) zal proberen elektronen te pakken en zoekt naar deeltjes die elektronen willen afstaan
(dat moeten dus reductoren zijn)
Als er dan deeltjes / stoffen in de elektroderuimten zijn die willen afstaan of opnemen - en dat mogen ook zwakke reductoren of oxidatoren zijn - dan zal dat ook gebeuren; als tenminste de externe stroombron voldoende sterk is.
Als die niet voldoende sterk is, dan kun je altijd het voltage opvoeren. Hoe zwakker de aanwezige oxidator of reductor, des te hoger voltage nodig is van de uitwendige stroombron.
Die oxidatoren en reductoren kunnen moleculen zijn, atomen of ionen, alles kan.
Let wel op: complexe ionen, vooral die ionen met zuurstof als sulfaat, hebben moeite met het meedoen aan dit soort elektrolysereacties wegens hun hoge activeringsenergie (waarop OH- weer een uitzondering is).
Ook hier weer: de redoxtabellen geven aan wie als reductor of oxidator zal optreden.
Opdracht 38
Een oplossing van calciumnitraat ondergaat elektrolyse met platina-elektroden.
Geef de vergelijkingen voor de twee halfreacties die aan de elektroden verlopen.
Bij elektrolyse verlopen de redox-halfreacties gescheiden en een totaalreactie is daarom niet altijd interessant of van belang.
Maar het wordt wel van belang als er berekeningen gedaan moeten worden:
- hoeveel moeten we oplossen?
- Hoeveel van dit of dat product kan er gevormd worden? Enzovoort.
In dat geval is een totaalreactie absoluut nodig.
Maar om de elektrolyse goed te begrijpen is het voldoende te weten wat er precies per elektrode gebeurt.
Opdracht 39
Stel dat je een stuk filtreerpapier hebt bevochtigd met een KI-oplossing waarin ook een paar druppels indicator (fenolftaleďne) zitten.
Twee elektroden aan een batterijtje breng je in contact met dit natte papier op ongeveer 1 cm afstand.
Er vindt dan een elektrolyse plaats (gedwongen redoxreactie).
- Geef de halfreacties
- Wat kun je hierbij waarnemen?
Elektroden maken indirecte redoxreacties mogelijk. De bijbehorende elektronenoverdracht gebeurt dus niet in direct contact tussen de reagerende deeltjes, maar via geleidend materiaal.
Ook bij elektrolyse kan de elektrode gemaakt zijn van inert materiaal (grafiet, platina) of hij doet mee aan de elektrolyse, zoals bijvoorbeeld als een elektrode gemaakt is van Zink of van Koper.
Denk er verder om dat ook hier de vloeistof tussen de elektroden geleidend moet zijn (moet vrije ionen bevatten).
Nog eens op een andere manier de elektrolyse uitgelegd:
Zeg dat de elektroden degenen zijn die de aanwezige deeltjes dwingen tot elektronenoverdracht.
De anode is positief, heeft dus tekort aan elektronen, wil graag elektronen opnemen, zoekt naar deeltjes in de buurt die elektronen kunnen afstaan en - bij voldoende voltage - dwingt deze elektrode die stof om dat ook te doen.
Bij de kathode gebeurt precies het omgekeerde.
Opdracht 40
- Formuleer precies wat er gebeurt aan de kathode.
- Zal de anode oxidatoren of reductoren naar zich toehalen? Leg je antwoord uit.
Opdracht 41
Kijk goed naar het volgende schema en leg het schema uit:
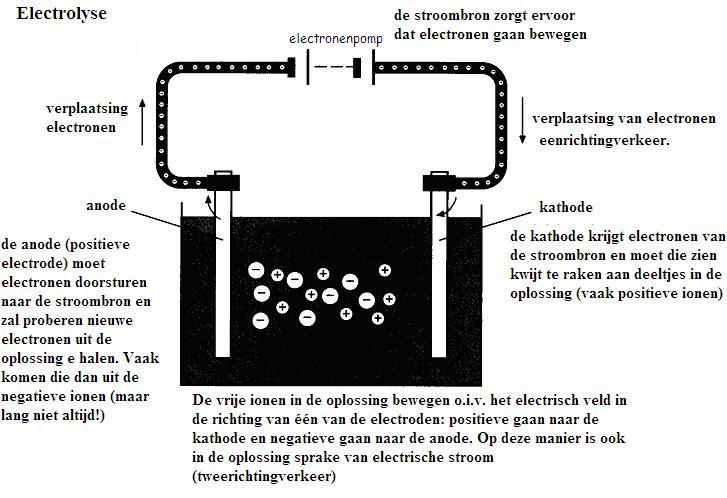
Een 'animatie':
Maak van de elektroden twee mensen: De handen van die twee mensen houden de stroombron vast, hebben daar contact en de man wordt volgestouwd met elektronen terwijl de vrouw leeggezogen wordt door diezelfde stroombron.
Ze voelen zich niet lekker, geen van beiden, en willen daar wat aan doen.
De man gaat nu optreden als de kathode en de vrouw wordt de anode:
De vrouw voelt groot gebrek aan elektronen en omdat ze met haar voeten in de oplossing staat gaat ze proberen daar elektronen uit te trekken, naar zich toe te halen. En jawel, ze ziet daar een of andere stof die elektronen kan afstaan (een reductor), doet er niet toe of die stof dat graag wil, maar ze dwingt die stof elektronen aan haar af te geven.
Dat gebeurt precies op het moment dat zo'n deeltje de voeten van de vrouw raakt.
De man voelt zich haast barsten van teveel aan elektronen, maar heeft nu eenmaal geen direct contact met de vrouw en staat alleen maar met zijn voeten in de oplossing waar wel een stofje is die elektronen kan overnemen (een oxidator), graag of niet.
Die stof wordt dan gedwongen tot elektronenovername om zo de man wat bevrediging en rust te geven.
Dat gebeurt zodra die deeltjes de voeten van de man aanraken.
Wat er gebeuren zou als de twee elektroden, man en vrouw, elkaar wel direct zouden tegenkomen laat zich raden.
Ernstige kortsluiting natuurlijk.
Opdracht 42
Probeer de elektrolyse uit te tekenen overeenkomstig bovenstaande animatie.
De galvanische cel uit onderstaande tekening ken je al.
De bedoeling van zo'n elektrochemisch element is het opwekken van elektrische energie met behulp van sterke chemische stoffen (oxidatoren en reductoren).
Altijd passen we twee redoxkoppels toe (vaak te vinden in de redoxtabel).
Je kunt de halfpotentiaal van een redoxkoppel meten en de waarden daarvan vind je in de meeste tabellen en die baseren zich dan op standaardomstandigheden: 25oC en 1 atm. gasdruk of een concentratie van 1M.
Hoe sterker een oxidator of reductor, des te hoger de geleverde halfpotentiaal.
Als je zo twee koppels samenvoegt tot een volledige cel, dan heb je tussen de twee redoxkoppels een potentiaalverschil. Bij een gewoon batterijtje is dat bijv. 1,5V.
Voorbeeld:
We hebben hier twee halfreacties van twee redoxkoppels:
Red: Cu Cu2+ + 2e-V(standaard) = +0,34 V
Cu2+ + 2e-V(standaard) = +0,34 V
Ox: Zn2+ + 2e-  Zn
Zn
V (standaard) = -0,76 V
Het potentiaalverschil, onder standaardomstandigheden, is: (red - ox) =0,34 - (-0,76) = 1,10 Volt [je moet altijd de kleinste van de grootste aftrekken]
Deze accu zal dus een voltage opleveren van 1,1 volt.
Als je de omstandigheden verandert, zal ook het potentiaalverschil veranderen. Een hogere concentratie aan zinkionen (meer OX) zal waarschijnlijk een hogere potentiaal opleveren.
Het oxidatiegetal is het aantal elektronen dat
- geheel of gedeeltelijk -
door een of ander deeltje wordt opgenomen of afgestaan.
Opdracht 43
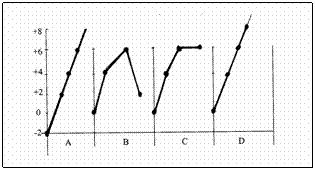
Het diagram hierboven toont de veranderende oxidatiegetallen van zwavel in het productieproces van zwavelzuur.
Het proces kan in grove lijnen als volgt worden aangegeven:
S  SO2
SO2  SO3
SO3
 H2SO4
H2SO4
Bewering: De grafiek D geeft als enige die veranderende oxidatiegetallen op de juiste wijze weer.
Leg uit of de bewering juist is of niet.
N.B.
- Neutrale elementen krijgen een oxidatiegetal met waarde 0 (de atomen hebben geen elektronen verloren of gewonnen).
- Waterstof als neutraal element heeft dus oxidatiegetal 0, maar in verbindingen is het vrijwel altijd +1.
- Zuurstof als neutraal element heeft oxidatiegetal 0, maar in verbindingen is het meestal -2.
Opdracht 44
Welke oxidatiegetallen hebben de elementen in de volgende stoffen:
Kaliumdichromaat; Natriumpermanganaat; Zilver; Water; Waterstofperoxide?
Opdracht 45
Welke van de volgende reacties zijn redoxreacties:
(leg je antwoord uit m.b.v. oxidatiegetallen)
- H2(g) + Br2(aq)
 2HBr(aq)
2HBr(aq)
- NH4NO3
 N2O+ 2H2O
N2O+ 2H2O
- NH4Cl
 NH3+ HCl
NH3+ HCl
- 2K2CrO4 + H2SO4
 K2Cr2O7+ K2SO4 + H2O
K2Cr2O7+ K2SO4 + H2O
- H3BO3 + 4HF
 HBF4+ 3H2O
HBF4+ 3H2O
- Fe(s) + S(s)
 FeS(s)
FeS(s)
Opdracht 46
Onderzoek m.b.v. de oxidatiegetallen wie in de volgende reacties oxidator of reductor is:
- SO2 + Br2 + 2H2O
 2HBr + H2SO4
2HBr + H2SO4
- Mg + H2SO4
 MgSO4 + H2
MgSO4 + H2
- Cu + 2H2SO4
 CuSO4 + SO2 + 2H2O
CuSO4 + SO2 + 2H2O
- 3I2 + 6KOH
 KIO3 + 5KI + 3H2O
KIO3 + 5KI + 3H2O
Antwoord 10-46
Het schema hieronder verdeelt de redoxreacties in drie (groene) vlakken, resultaat van het samengaan van directe, indirecte redox met zwakke en sterke stoffen.
Dat levert spontane en gedwongen redoxreacties op:
|
|
Direct
|
Indirect
|
|
sterk
|
spontane reacties
|
batterijen & accu's
aan het werk
|
|
zwak
|
er gebeurt niets
effectiefs
|
elektrolyse en
opladen van
batterijen en accu's
|
Als we redoxreacties willen oplossen, niet met oxidatiegetallen, maar met de halfreactievergelijkingen, volgen we een aantal regels:
- over welke reactie gaat het?
- welke deeltjes doen mee?
- wat zijn de half-vergelijkingen?
- wat is de totaalreactievergelijking?
- welke conclusies kunnen we trekken en waarnemingen kunnen we doen?
Het volgende schema toont 6 stappen die altijd terugkomen bij het oplossen van redoxreacties, hier en daar een beetje
afhankelijk of het een directe (geen elektroden) of indirecte reactie (met elektroden) is.
|
Zonder elektroden
|
Met elektroden
|
|
1. maak een schets van wat er allemaal gebeurt / gedaan wordt.
|
|
2a. Maak een lijst van alle aanwezige stoffen / deeltjes, inclusief elektroden)
2b. Geef aan wat de reductor en wat de oxidator is(onderstrepen)
|
|
|
3. geef de halfreactievergelijkingen
|
3. geef de halfreactievergelijkingen
OX reageert aan de positieve elektrode
RED reageert aan de negatieve elektrode
|
|
4. kloppend maken en totaalvergelijking
|
4. kloppend maken van elektrodereacties
|
|
5. noteer eventuele volgreacties
|
|
|
6. Noteer waarnemingen en conclusies
|
|
N.B.: het gebruik van de redoxtabel is onmisbaar.
Een voorbeeld:
In het chemisch lab brengen we een klein stukje van het metaal natrium in gedestilleerd water (doen we in een soort aquarium).
Het Natrium is een zacht metaal waar we gewoon een stukje vanaf kunnen snijden of knippen, maar voorzichtig:
het wordt niet voor niets onder petroleum bewaard; het reageert spontaan met luchtzuurstof en met water.
Het afgeknipte stukje natrium drogen we (met filtreerpapier halen we het petroleum er af)
en we leggen het voorzichtig op het wateroppervlak.
Meteen begint het hevig te reageren, er vormt zich een gas, het stukje natrium gaat snel bewegen over het wateroppervlak, al brandend met gele vlammen.
Dat gaat door tot het metaal helemaal verdwenen is.
Een paar druppels indicator toevoegen aan het water laat zien dat het gedestilleerd water basisch is geworden.
Dit is duidelijk een directe reactie: de natriumdeeltjes botsen direct met de waterdeeltjes en er zijn geen elektroden.
De reactie is zeer spontaan.
We volgen de zes stappen:
- Een situatieschets:
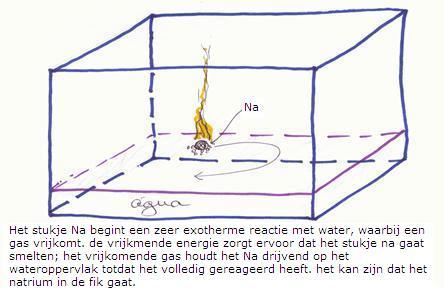
- de aanwezige deeltjes/stoffen zijn: natrium en water, verder niets.
Kijken we in de tabel, dan moeten we concluderen dat water zowel als oxidator en als reductor kan optreden (in beide gevallen zeer zwak).
Maar natrium daarentegen is een zeer sterke reductor, dus logisch om te denken dat het water in dit geval als oxidator gaat optreden.
De reductor staat hier lager dan de oxidator, dus de reactie is spontaan.
- De halfreactievergelijkingen:
| Red: |
Na |
 |
Na+ + e- |
|x2 |
| Ox: |
2H2O + 2e- |
 |
H2 + 2OH- |
|x1 |
NB: het aantal elektronen moet in beide halfreacties gelijk zijn
- De totaalreactievergelijking:
2Na + 2H2O  2Na+ + H2 + 2OH-
2Na+ + H2 + 2OH-
of:
2Na(s) + 2H2O(l) 2NaOH(aq) + H2(g) ΔH < 0
2NaOH(aq) + H2(g) ΔH < 0
- Waarschijnlijk is hier één vervolgreactie: het waterstofgas dat ontstaat is verantwoordelijk voor de brand; het reageert met zuurstof uit de lucht en veroorzaakt de vlammen.
- Waarnemingen en conclusies:
- De reactie is spontaan, er komt energie vrij in de vorm van warmte en licht; het is dus exotherme reactie.
- Er vormt zich het gas waterstof dat gemakkelijk ontvlamt en zal branden; dat is te zien.
- Het product NaOH creëert een basisch milieu (ionen OH-); dat kunnen we controleren met de indicator: kleur wordt violet.
Opdracht 47
Hieronder 6 redoxreacties om op te lossen volgens de 6 regels van het schema.
- Calcium(s) met water(l)
- Koper(s) met geconcentreerd salpeterzuur
- Kaliumpermanganaat(aq) met oxaalzuur(aq) (in aanwezigheid van verdund zwavelzuur)
- Koper(s) met zinksulfaat(aq)
- Broom(aq) met Kaliumjodide(aq)
- Kaliumpermanganaat(aq) met natriumsulfiet(aq)
Opdracht 48
- Wat kun je waarnemen bij de reactie van kalium met water?
- Zal deze reactie meer of minder hevig zijn, in vergelijking met natrium?
In deze module gaan we niet uitvoerig in op toepassingen omdat daarvoor een aparte module gemaakt wordt (module 15).
Maar een paar voorbeelden van redox in de praktijk laten we hier wel zien: het gaat om "blazen bij verkeerscontrole" en de ouderwetse zwart-wit fotografie.
Ofwel: wie 'bobt' er vandaag?
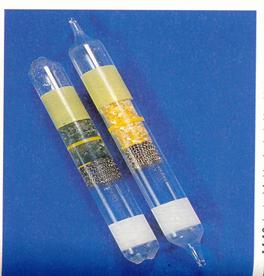
De opgenomen alcohol komt in het bloed terecht en deels in de longen en andere organen (ook hersenen) en zal het reactievermogen van de chauffeur aantasten. Bij ongelukken heeft de gedronken chauffeur automatisch schuld. De politie heeft verschillende mogelijkheden om te controleren; één daarvan is gebaseerd op de redoxreacties: het blaaspijpje.
Daarin bevindt zich kaliumdichromaat in zuur milieu met een gele kleur. Als bij het blazen de alcohol geoxideerd wordt door het bichromaat, ontstaat er een groengekleurde stof (met Cr(III)-ionen). Als dat gebeurt zal de agent je niet door laten rijden. Het andere product dat hierbij ontstaat is azijnzuur.
Opdracht 49
- Vind je deze controle nuttig en rechtvaardig, wetenschappelijk, maar ook moreel gezien?
- Geef de halfreactievergelijkingen en een totaalvergelijking en leg aan de hand daarvan de waarnemingen uit.
Fotografen en hobbyisten drukten vroeger in hun donkere kamer hun eigen (zwart-wit)-foto's af op fotografisch papier. Bestaat nog!!
Dat papier bevat een laag van zeer fijne kristallen zilverbromide.
Op het moment dat lichtstraling (energie) zo'n kristal bereikt wordt het in zekere zin aangetast:
AgBr(s)  Ag(s) + Br2(g)
Ag(s) + Br2(g)
Ag(s) is zwart, en Br2
(ontsnapt in gasvorm)
Op het papier zie je nog niets van dit proces, direct na de belichting, maar die aantasting heeft wel op allerlei plekken plaats gevonden.
Dan moet je dat papier vervolgens in een ontwikkelbad onderdompelen (1). Elk aangetast kristal (heeft al een beetje neutraal zilver) zal gaan reageren met de stoffen in dat bad: hydroxide en dihydroxibenzeen
2AgBr(s) + 2KOH(aq) + H2O + OH-  2Ag(zwart) + andere stoffen
2Ag(zwart) + andere stoffen
Hoe meer licht op de kristallen viel, des te meer zilver zal verschijnen en des te zwarter het resultaat.
Dan is er nog een heleboel ongebruikt zilverbromide over en dat mag natuurlijk niet daar blijven zitten. Dat zou alleen maar problemen veroorzaken als de film of het fotopapier daarna in het licht komt.
Het overbodige en overgebleven zilverbromide moet weg en daarvoor gebruikt men "fixeer", een oplossing van ammoniumtiosulfaat.
AgBr(s) + 2(NH4)2S2O3(aq)  NH4Br(aq) + (NH4)3(AgS4O6)(aq)
NH4Br(aq) + (NH4)3(AgS4O6)(aq)
Tenslotte is het alleen nog maar een kwestie van het papier of de film drogen.
Opdracht 50
Controleer van alle reacties van 6.2 de veranderingen in oxidatiegetallen
 Koper(s) + IJzer(II)sulfaat(aq)
Koper(s) + IJzer(II)sulfaat(aq)

 Koper(s) + IJzer(II)sulfaat(aq)
Koper(s) + IJzer(II)sulfaat(aq)
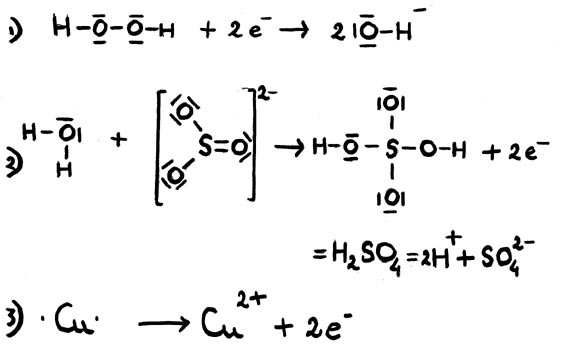









 ox1 + red2
ox1 + red2



 NO2 + H2O
NO2 + H2O
 NO + 2H2O
NO + 2H2O
 N2 + 6H2O
N2 + 6H2O
 N2O + 5H2
N2O + 5H2
 ox 1 + red 2
ox 1 + red 2


 Au
Au
 NO2 + H2O
NO2 + H2O
 Ag
Ag
 Fe2+
Fe2+
 Cu
Cu
 Cu+
Cu+
 SO32- + H2O
SO32- + H2O
 Pb
Pb
 Ni
Ni
 Pb + SO42-
Pb + SO42-
 Fe
Fe
 Zn
Zn
 H2 + 2OH-
H2 + 2OH-
 Al
Al
 Mg
Mg
 Al + 4OH-
Al + 4OH-
 Na
Na
 Ba
Ba
 Ca
Ca
 K
K


 2H2O
2H2O
 O2 +2H+ + 2e-
O2 +2H+ + 2e-







 Zn2+ + 2e-
Zn2+ + 2e-
 Cu(s)
Cu(s)


 Fe2++2e-
Fe2++2e-

 ox1 (Cu2+) + elektronen (a)
ox1 (Cu2+) + elektronen (a)
 red2 (Zn) (b)
red2 (Zn) (b)


 Cu2+ + 2e-V(standaard) = +0,34 V
Cu2+ + 2e-V(standaard) = +0,34 V
 Zn
Zn

 SO2
SO2  SO3
SO3
 H2SO4
H2SO4
 2HBr(aq)
2HBr(aq)
 N2O+ 2H2O
N2O+ 2H2O
 NH3+ HCl
NH3+ HCl
 K2Cr2O7+ K2SO4 + H2O
K2Cr2O7+ K2SO4 + H2O
 HBF4+ 3H2O
HBF4+ 3H2O
 FeS(s)
FeS(s)
 2HBr + H2SO4
2HBr + H2SO4 MgSO4 + H2
MgSO4 + H2 CuSO4 + SO2 + 2H2O
CuSO4 + SO2 + 2H2O KIO3 + 5KI + 3H2O
KIO3 + 5KI + 3H2O


 2Na+ + H2 + 2OH-
2Na+ + H2 + 2OH-
 2NaOH(aq) + H2(g) ΔH < 0
2NaOH(aq) + H2(g) ΔH < 0

 Ag(s) + Br2(g)
Ag(s) + Br2(g)
 2Ag(zwart) + andere stoffen
2Ag(zwart) + andere stoffen
 NH4Br(aq) + (NH4)3(AgS4O6)(aq)
NH4Br(aq) + (NH4)3(AgS4O6)(aq)