Spectrometrie
Als je aan de deeltjes van een stof (atomen, ionen, moleculen) extra energie toevoegt door ze bijvoorbeeld te verhitten of te bestralen dan kan de stof een deel van die energie opnemen.
Waar blijft die energie? (want: "energie gaat nooit verloren, toch?")
Die opgenomen energie kan op verschillende manieren in zo'n deeltje terechtkomen en worden opgeslagen:
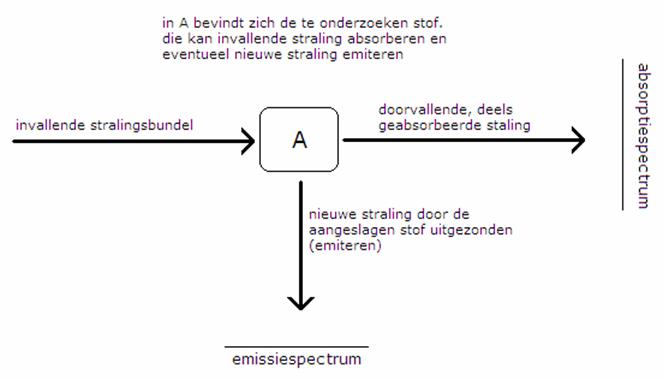
Er zijn twee soorten spectra te onderscheiden:
De aangeslagen moleculen zijn niet stabiel en zullen (snel) terugvallen in de grondtoestand. Bij dat terugvallen wordt nieuwe straling uitgezonden (in alle richtingen). Ook deze emissiestraling kan met een detektor (in de tekening onder een hoek van 90 graden) worden gemeten en in een grafiek worden uitgezet. Je ziet pieken naar boven.
Aan het patroon van een spectrum is vaak te herkennen om welk molecuul het gaat. Het zijn een soort vingerafdrukken van moleculen en atomen.
Als je aan de deeltjes van een stof (atomen, ionen, moleculen) extra energie toevoegt door ze bijvoorbeeld te verhitten of te bestralen dan kan de stof een deel van die energie opnemen.
Waar blijft die energie? (want: "energie gaat nooit verloren, toch?")
Die opgenomen energie kan op verschillende manieren in zo'n deeltje terechtkomen en worden opgeslagen:
- De energie wordt opgenomen door de elektronen van een bepaald atoom.
Hoe meer energie elektronen bezitten, des te "zelfstandiger" ze zijn;
met andere woorden:
Hoe verder elektronen van de kern zijn verwijderd, des te meer ze 'op zichzelf' kunnen zijn en des te meer eigen energie hebben ze.
Als dus die toegevoerde (voldoende) energie bij de elektronen terechtkomt, dan zullen die elektronen overspringen naar een verder van de kern liggende schil (zie B).
Zelfs is het mogelijk dat zo'n elektron zoveel energie verkrijgt dat het het atoom verlaat; er ontstaat dan een positief ion (zie A).- Eén of méér elektronen nemen zoveel energie op dat ze zich volledig verwijderen van het atoom; dit heet ionisatie en levert geen spectrum op.
- Eén elektron neemt energie op gaat daardoor naar een verder naar buiten gelegen schil. De energie zit nu dus nog in het atoom, dat daardoor niet stabiel is. Hoe meer energie een deeltje heeft, des te onstabieler is het.
Dat onstabiele deeltje bevindt zich in de zgn. AANGESLAGEN TOESTAND. Elektronen met teveel aan energie zullen snel (binnen frakties van een sekonde) weer terugvallen in hun oorspronkelijke stabiele GRONDTOESTAND.
Dat terugvallen kan eventueel in etappes, via tussenliggende (onder)schillen, plaats vinden. Bij elk terugsprongetje moet dat elektron overtollige energie afgeven in de vorm van elektromagnetische straling van bepaalde golflengte.
De manier waarop elektronen terugvallen is voor elk atoom verschillend, dus ook de uitgezonden straling is dan verschillend. Die uitgezonden straling kan opgevangen en gemeten worden; soms zelfs met het blote oog te zien als de golflengte tussen de 400 en 700 nm ligt.
- De energie wordt opgenomen door de moleculen.
Binnen moleculen zijn de atomen ten opzichte van elkaar in trilling, elk molecuul en elk atoom op zijn eigen manier. Als de toegevoerde energie niet groot genoeg is om elektronen naar een andere schil te sturen, dan komt deze mogelijkheid ter sprake. Vaak worden daarvoor de moleculen met infraroodlicht bestraald. Als het molecuul de energie van die straling (gedeeltelijk) kan opnemen zal het bijvoorbeeld wat heviger of in een andere richting gaan trillen en geraakt ook op die manier in een soort aangeslagen toestand, die weer niet stabiel is. Het aangeslagen molecuul zal snel weer terugvallen in de oorspronkelijke grondtoestand onder uitzenden van nieuwe straling. Deze nieuwe straling kan weer gemeten worden met spectrometers en daaruit kunnen dan conclusies getrokken worden omtrent de aard van de onderzochte stof.
- De energie wordt opgenomen door de atoomKERN.
Ook de kerndeeltjes zijn in staat bepaalde energie op te nemen en even later weer af te staan. En ook dit levert een spectrum op (NMR). Hierbij speelt het magnetisch veld een belangrijke rol.

Er zijn twee soorten spectra te onderscheiden:
- Een absorptiespectrum
- Een emissiespectrum
De aangeslagen moleculen zijn niet stabiel en zullen (snel) terugvallen in de grondtoestand. Bij dat terugvallen wordt nieuwe straling uitgezonden (in alle richtingen). Ook deze emissiestraling kan met een detektor (in de tekening onder een hoek van 90 graden) worden gemeten en in een grafiek worden uitgezet. Je ziet pieken naar boven.
Aan het patroon van een spectrum is vaak te herkennen om welk molecuul het gaat. Het zijn een soort vingerafdrukken van moleculen en atomen.