Kw
Waterconstante
Water zelf is een zwak amfolyt, dus een zeer zwakke base Õn een zeer zwak zuur.
Als er in water geen andere stoffen zijn opgelost, dan is de pH van dat water bij 25 graden precies 7 en ook de pOH = 7.
Bij het waterevenwicht (H2O + H2O H3O+ + OH-) behoort uiteraard ook een evenwichtsvoorwaaarde K:
H3O+ + OH-) behoort uiteraard ook een evenwichtsvoorwaaarde K:
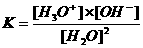
De waterconcentratie is constant = Ý55,5 mol/l is
De watersplitsing verandert daaraan praktisch niets.
K.[H2O]2 = [H3O+].[OH-] K·55,5 = Kw = 10-7·10-7 = 10-14
K·55,5 = Kw = 10-7·10-7 = 10-14
Kw noemt men de waterconstante en is bij 25°C : 10-14
Zoals alle evenwichtsconstanten is ook de waterconstante alleen afhankelijk van de temperatuur.
De bovenstaande formules kun je ook m.b.v. p-waarden opschrijven:
pKw = pH + pOH
of in getallen:
pKw = 14 = 7 + 7
Als de pH en de pOH aan elkaar gelijk zijn, dus de [H3O+] en de [OH-] zijn aan elkaar gelijk, dan is de oplossing neutraal.
Omdat Kw een constante is (dus pKw ook) moeten pH en pOH samen altijd 14 zijn
bijvoorbeeld: pH = 5 en pOH = 9. [let op: alleen bij kamertemperatuur!]
Als de pH groter wordt, dan wordt de pOH kleiner en v.v.
Water zelf is een zwak amfolyt, dus een zeer zwakke base Õn een zeer zwak zuur.
Als er in water geen andere stoffen zijn opgelost, dan is de pH van dat water bij 25 graden precies 7 en ook de pOH = 7.
Bij het waterevenwicht (H2O + H2O
 H3O+ + OH-) behoort uiteraard ook een evenwichtsvoorwaaarde K:
H3O+ + OH-) behoort uiteraard ook een evenwichtsvoorwaaarde K:
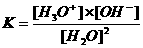
De waterconcentratie is constant = Ý55,5 mol/l is
De watersplitsing verandert daaraan praktisch niets.
K.[H2O]2 = [H3O+].[OH-]
 K·55,5 = Kw = 10-7·10-7 = 10-14
K·55,5 = Kw = 10-7·10-7 = 10-14
Kw noemt men de waterconstante en is bij 25°C : 10-14
Zoals alle evenwichtsconstanten is ook de waterconstante alleen afhankelijk van de temperatuur.
De bovenstaande formules kun je ook m.b.v. p-waarden opschrijven:
pKw = pH + pOH
of in getallen:
pKw = 14 = 7 + 7
Als de pH en de pOH aan elkaar gelijk zijn, dus de [H3O+] en de [OH-] zijn aan elkaar gelijk, dan is de oplossing neutraal.
Omdat Kw een constante is (dus pKw ook) moeten pH en pOH samen altijd 14 zijn
bijvoorbeeld: pH = 5 en pOH = 9. [let op: alleen bij kamertemperatuur!]
Als de pH groter wordt, dan wordt de pOH kleiner en v.v.
- Door toevoeging van zuur wordt de [H3O+] groter, dus de pH <.
- Door toevoeging van base wordt de [OH-] groter, dus de pOH <.