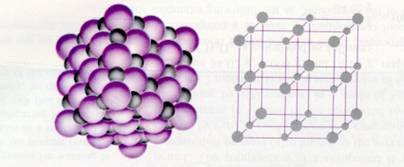
Die grotere paarse bolletjes stellen dan bijvoorbeeld de negatieve ionen voor en de grijze, kleinere bolletjes staan voor de positieve metaalionen.
Stoffen die uit ionen zijn opgebouwd vormen IONROOSTERS.
De verschillende ionen gaan zich netjes rangschikken.
Positieve ionen zijn omgeven door negatieve en negatieve ionen zijn omgeven door positieve (allemaal vanwege die aantrekkingskracht natuurlijk).
Die roosters zitten door al die aantrekkingskrachten erg stevig in elkaar.
Het is handig om alvast te weten dat de meeste stoffen met een ionrooster zouten genoemd worden.
Als stoffen uit ionen zijn opgebouwd, vormen ze geen moleculen.
Stoffen met ionbindingen zijn neutraal, maar alleen omdat er evenveel negatieve als positieve ladingen in zitten.
Positieve en negatieve ionen gaan altijd zo bij elkaar zitten dat in totaal een neutrale stof ontstaat: met evenveel positieve als negatieve lading.
Dus:
In zouten heb je sterke aantrekkingskrachten tussen positieve en negatieve ionen.
Deze inter-ionaire krachten bepalen de sterkte van het rooster en dus ook het smeltpunt. Doorslaggevend hierbij zijn de lading van de ionen en de afstand tussen de ionen (d.w.z. die wordt bepaald door de ionstralen). Een sterk rooster heeft kleine ionen met hoge lading.
Zo heeft bijvoorbeeld MgO een veel sterker ionrooster dan NaCl, omdat de magnesium en zuurstofionen kleiner zijn en sterker geladen dan de natrium en chloride-ionen.
In zo'n ionrooster zitten de positieve en negatieve ionen netjes gerangschikt. Daarbinnen heersen dus altijd sterke ladingskrachten.
Kenmerken: kristallijn, hoog smeltpunt, als vloeistof (dus in gesmolten toestand) geleidend. De kristallen echter geleiden niet!
De positieve en negatieve ionen gaan in een bepaalde vaste verhouding in ongelooflijk grote hoeveelheden en netjes gerangschikt bij elkaar zitten in Het IONROOSTER.
De verhouding waarin die ionen bij elkaar gaan zitten wordt aangegeven d.m.v. cijfertjes rechtsonder, alsof het een molecuulformule is, maar eigenlijk is het een VERHOUDINGSFORMULE.
Let op: op het eerste gezicht lijkt er geen verschil tussen verhoudingsformule en molecuulformule.