De molecuulformule van benzeen is: C6H6
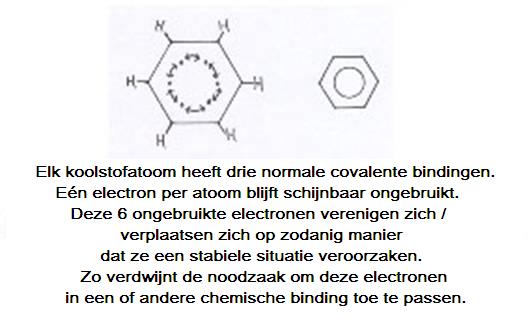
De benzeenring kun je opvatten als opgebouwd uit zes koolstofatomen, die elk drie van hun valentie-elektronen gebruiken voor bindingen met één H en twee buur-C's.
Elk koolstofatoom in de ring heeft drie normale covalente bindingen. Zo blijft elk C-atoom nog zitten met een 'niet gepaard elektron' dat nog kan koppelen met welk ander atoom dan ook.
In totaal dus 6 elektronen in voorraad, en deze zes gaan nu op een bijzondere manier met elkaar, dus zonder andere atomen, een speciale π-binding (een "pi-binding) vormen. Daar komen we later uitvoerig op terug.
We behandelen hier niet de meer ingewikkelde bindingstypes, dus je mag de zaak hier versimpelen door te zeggen:
Die zes elektronen verkrijgen de gelegenheid om zich te verplaatsen over die ring van 6 atomen.
Ze mogen zich dus vrij over die ring bewegen en verkrijgen daardoor grote beweeglijkheid.
Dat betekent tegelijk: die ring wordt veel stabieler daardoor.
Als moleculen (uit de koolstofchemie) dit soort ringstructuren hebben met elektronenverplaatsing, dan spreken we van aromatische moleculen.

De benzeenring kun je opvatten als opgebouwd uit zes koolstofatomen, die elk drie van hun valentie-elektronen gebruiken voor bindingen met één H en twee buur-C's.
Elk koolstofatoom in de ring heeft drie normale covalente bindingen. Zo blijft elk C-atoom nog zitten met een 'niet gepaard elektron' dat nog kan koppelen met welk ander atoom dan ook.
In totaal dus 6 elektronen in voorraad, en deze zes gaan nu op een bijzondere manier met elkaar, dus zonder andere atomen, een speciale π-binding (een "pi-binding) vormen. Daar komen we later uitvoerig op terug.
We behandelen hier niet de meer ingewikkelde bindingstypes, dus je mag de zaak hier versimpelen door te zeggen:
Die zes elektronen verkrijgen de gelegenheid om zich te verplaatsen over die ring van 6 atomen.
Ze mogen zich dus vrij over die ring bewegen en verkrijgen daardoor grote beweeglijkheid.
Dat betekent tegelijk: die ring wordt veel stabieler daardoor.
Als moleculen (uit de koolstofchemie) dit soort ringstructuren hebben met elektronenverplaatsing, dan spreken we van aromatische moleculen.